
2月9日,浙江大学医学院附属妇产科医院(以下简称浙大妇院)主任医师、教授汪辉团队的“宫颈癌精准筛查与防治关键技术创新及推广”技术成果,获得2024年度浙江省科学技术进步奖一等奖。
宫颈癌是全球女性第四大常见恶性肿瘤,被称为“女性健康的杀手”。据测算,我国每年约有4500万名适龄女性感染高危HPV(人乳头瘤病毒),年均宫颈癌新发病例达15.1万,且呈年轻化趋势。
为了消除这一“女性健康杀手”,世界卫生组织提出加速消除宫颈癌的全球战略。我国也提出,到2030年我国适龄妇女宫颈癌筛查率目标达到70%,宫颈癌及癌前病变患者治疗率达到90%。
“消除”二字谈何容易?致病机制不清,HPV疫苗接种率不高,传统筛查精度不足和覆盖率不高,常规治疗手段很多时候要以牺牲子宫、卵巢为代价……
汪辉带领团队围绕宫颈癌“为何发、如何筛、怎样治”三大核心命题,历时数十年进行科研攻坚,构建起“理论创新—技术突破—产品转化—临床应用”的全链条原创成果体系。
如今,项目关键技术已在四川大学华西医院、中南大学湘雅医院等全国500余家医疗机构推广应用,服务患者超70万人次。

图为浙江大学医学院附属妇产科医院主任医师、教授汪辉获奖留影。
打开“盲盒” 揭开HPV整合致癌神秘面纱
“医生,我HPV检查出来阳性,是不是得宫颈癌了?”作为国内顶尖的妇科肿瘤专家,汪辉经常碰到患者拿着报告单来门诊咨询。
其实,HPV阳性并不等于宫颈癌,高危HPV持续感染才是宫颈癌的主要病因。但一个令人困惑的现象:女性HPV感染率约15%,仅1%的高危人群最终发展为宫颈癌。从感染到癌变,这中间究竟发生了什么?到底哪些才是真正的宫颈癌高危人群?
此前的科学家们发现,HPV整合,即进入人体后的HPV病毒“长”到人体基因中,是宫颈癌变的关键一步。HPV整合是怎样形成的?整合又是如何导致癌症发生的呢?这两个核心问题始终悬而未决,直接导致了无法精准甄别宫颈癌高危人群、阻断病变进展。
“我们怀疑其中很可能存在关键的调控机制。”汪辉决心从源头破解致癌密码。
为了打开癌变“盲盒”,团队耗时数年鉴定了全球数量最多的宫颈癌HPV感染整合位点,共3667个,并最终绘制出首份HPV高频整合位点图谱。

图为HPV高频整合位点图谱。
据此,团队首次提出了“微同源介导HPV整合驱动宫颈癌”新理论。
通俗地讲,HPV病毒进入体内后,像一个“潜伏者”按兵不动,当人体基因受外界刺激等原因产生断裂时,HPV病毒就“浮出水面”,只要病毒基因和人体基因在断裂处附近存在一小段碱基互补配对的序列,也就是“微同源序列”,HPV基因就能成功嵌入人体基因组,并像“搭积木”一样连在一起。
“癌变的前提是整合,而这些断裂的地方正好给整合提供了条件。”汪辉进一步解释,“宫颈的鳞柱交界部是细胞不断脱落、生长的区域,不成熟的新生宫颈细胞容易受外界不良刺激影响,导致基因发生断裂,而HPV病毒就是在这个时候‘乘虚而入’。”
整合之后又发生了什么呢?团队进一步深挖机制,发现HPV整合不仅会导致宫颈上皮细胞抑癌基因和癌基因表达失控从而发生恶变,还会通过驱动巨噬细胞HK3/mTOR通路,抑制CD8+T细胞功能,从而促进肿瘤免疫逃逸。该发现完整揭示了宫颈病变进展的内在机制及外周免疫抑制特征,为后续诊疗技术研发指明了方向。
该理论获得国际学界的广泛认可。密歇根大学教授Glover TW在《Nature Reviews Cancer》中评述:“HPV整合开创了病毒致癌机制研究新方向。”美国医学遗传学会创始人Gollin SM教授在HPV相关肿瘤权威专著中大篇幅收录“微同源介导HPV整合”原创理论;日本京都大学教授Seishi Ogawa也在《Nature》论著中论证并引用汪辉团队的发现……
精准筛查 甄别“真危险”与“假警报”
从机制上厘清了宫颈癌“为何发”,团队把目标对准了“如何筛”。
宫颈癌筛查长期面临着“守不住”“守太严”的双重问题:传统细胞学检查假阴性率高,漏诊风险大;高危HPV16/18型阳性者需100%转诊相关活检,导致大量低风险人群承受了不必要的创伤与焦虑。
为了更好判断“真危险”与“假警报”,团队以HPV整合理论为核心,打造了一套筛查技术体系,其核心就是全球首个HPV整合检测试剂盒的诞生。试剂盒能精准检测出所有HPV整合位点,让诊断宫颈上皮内瘤变3级以上(CIN3+)的特异性较传统细胞学检查提升近20%。
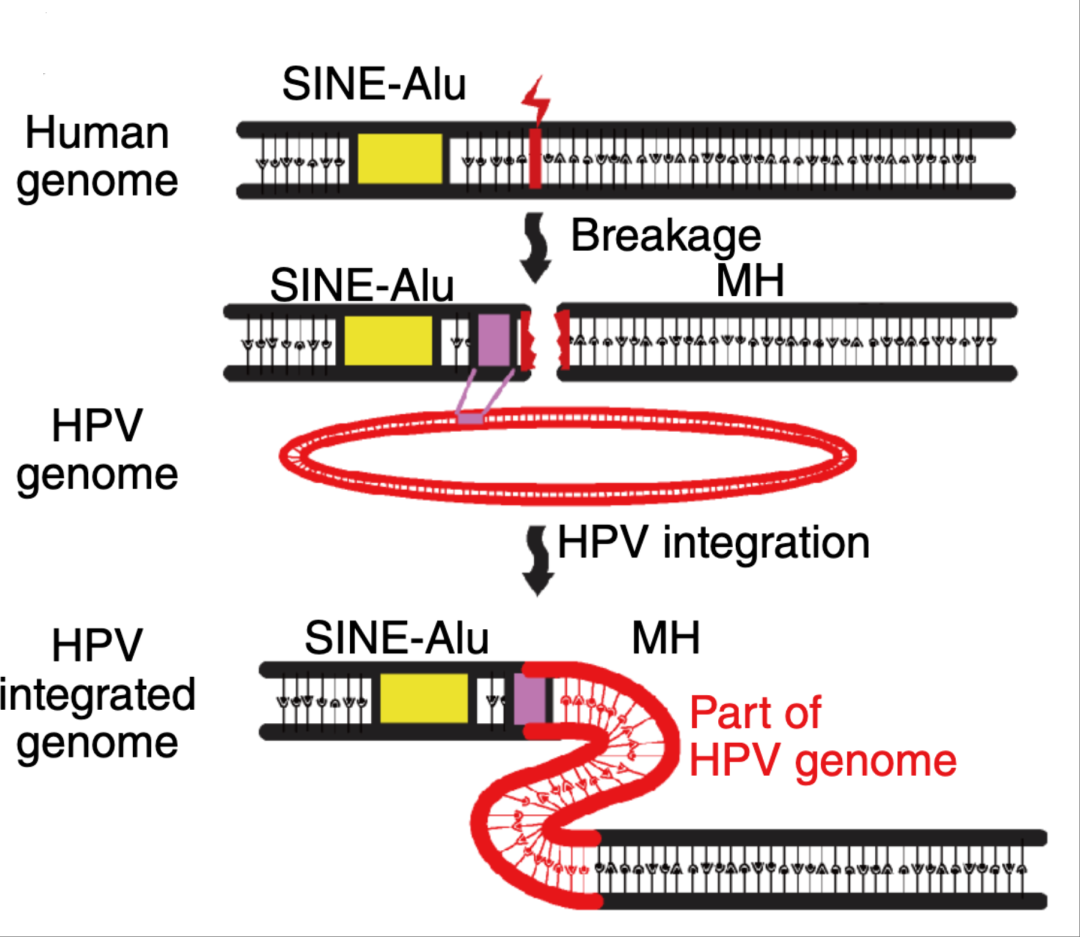
微同源介导修复示意图。浙大妇院供图
“我们通过医院人群和普通筛查人群的队列研究,首次证实HPV整合阳性者宫颈病变进展风险较阴性者增加5.6倍。”浙大妇院主任医师、教授李晓介绍,HPV16/18阳性但整合阴性的人,诊断为宫颈高级别病变的风险只有3.2%,这意味着成果应用后将避免大多数人群遭受相关活检带来的创伤。
试剂盒在2022年正式获批,目前在全国30余家三甲医院应用。
针对中国宫颈癌基层筛查条件有限的现状,团队还研发了我国首个基于杂交捕获技术的HPV筛查试剂盒。该试剂盒能精准分出HPV16/18型,检测效能与国际主流产品持平。
传统的宫颈刮片或相关检查带来的不适和尴尬,让不少女性望而却步,直接影响了宫颈癌筛查的覆盖率。团队从女性需求出发,首创了基于外周免疫特征的非侵入性诊断技术。
团队运用单细胞技术进行深度分析,发现随着宫颈病变程度加重,血液中某些免疫细胞(如CD4+T细胞)的比例会规律性升高,而另一些细胞(如CD8+T细胞等)则会减少。同时,团队成功定位到与高级别癌前病变(CIN2+)特异性关联的一系列免疫特征。
非侵入性诊断技术只需抽取患者静脉血,利用人工智能模型对血液中的免疫细胞图谱进行分析,就能判断受检者患有高级别宫颈癌前病变的风险。
临床验证显示,这项“滴血识风险”的新技术,对于CIN2+的检出灵敏度相比传统细胞学检查提升了约50%。
“三保”方案 守护女性生育力与家庭希望
传统宫颈癌的治疗存在三大弊端:宫颈癌前病变行宫颈锥切术易导致宫颈机能不全,患者容易因“宫颈门关不牢”引发流产、早产;宫颈癌根治术常需切除子宫,患者失去生育能力;高复发风险患者术后放化疗会摧毁卵巢功能。
“宫颈癌患者是一个个渴望活下去、活得好的女性。尤其育龄患者,保留生育能力不仅是生理功能完整,更是守护一个家庭的希望与未来。”汪辉说。
带着这份初心,团队研发了“保宫颈、保子宫、保卵巢”的功能保护治疗新方案。
在癌前病变治疗领域,团队首次将分子编辑技术应用于靶向HPV癌基因,成功逆转宫颈病变,同时将传统阴道栓剂升级为分子靶向递送系统,治愈率达80%。“这样一来,癌前病变的患者就不需要进行手术治疗,有效保护了育龄女性的宫颈机能。”浙大妇院主任医师、教授程晓东说。
针对早期宫颈癌患者,团队提出了新辅助化疗结合宫颈锥切或广泛宫颈切除术的个性化方案,打破了“宫颈癌必须切除子宫”的传统认知,为患者保留生育能力奠定基础。
确诊为局部晚期宫颈癌的林女士(化名),年仅28岁,渴望成为母亲。来浙大妇院就诊后,团队为其量身定制个性化治疗方案,成功保住了子宫,守住了成为妈妈的美好可能。
对于术后存在高复发风险的年轻患者,团队通过牵头多中心临床研究,首次证实了单纯辅助化疗与同步放化疗疗效相当,且能维持正常雌激素水平,完整保留卵巢功能。
目前,“保宫颈、保子宫、保卵巢”的功能保护治疗新方案被写入《妇产科学》教材和多项指南共识,正在成为行业可复制、可推广的标准路径。诺贝尔化学奖获得者Jennifer AD教授评价说:“这项工作开拓了生物治疗病毒所致肿瘤的新时代。”
科技日报记者 江耘 通讯员 李晟曈 吴雅兰

浙公网安备 33010202000574号
版权所有:浙江大学医学院附属妇产科医院 浙ICP备05080900号-1
Copyright © 2016 Women's Hospital School Of Medicine Zhejiang University